Asam Amino
Asam Amino Adalah – Pengertian, Makalah Penggolongan Dan Sifatnya – Dalam hal ini mendengar kata asam amino yang terlintas pada pikiran sebagian orang ialah protein. Asam amino memang merupakan bagian protein dari gugus amina yang memiliki peran penting dalam pertumbuhan tubuh dan perkembangan otak manusia.
Latar Belakang
Biokimia merupakan ilmu yang mempelajari struktur dan fungsi komponen selular, seperti protein, karbohidrat, asam lemak, minyak, dan biomolekul lainnya.
Sekitar 75% asam amino digunakan untuk sintesis protein. Asam-asam amino dapat diperoleh dari protein yang kita makan atau dari hasil degradasi protein di dalam tubuh kita. Protein yang terdapat dalam makanan di cerna dalam lambung dan usus menjadi asam-asam amino yang diabsorpsi dan di bawa oleh darah ke hati. Protein dalam tubuh dibentuk dari asam amino.
Bila ada kelebihan asam amino akan di ubah menjadi asam ketogkutarat yang dapat masuk kedalam siklus asam sitrat. Hati adalah organ tubuh dimana terjadi reaksi Anabolisme dan Katabolisme. Proses Metabolik dan katabolik juga terjadi dalam jaringan di luar hati. Asam amino yang terdapat dalam darah berasal dari tiga sumber yaitu absorpsi melalui dinding usus, hasil penguraian protein dalam sel dan hasil sintesis asam amino dalam sel. Hati berfungsi sebagai pengatur konsentrasi asam amino dalam darah.
Asam amino adalah asam karboksilat yang mempunyai gugus amino. Asam amino yang terdapat sebagai komponen protein mempunyai gugus –NH2 pada atom karbon α dari posisi gugus –COOH. Jenis-jenis asam amino, urutan cara asam amino tersebut terangkai, serta hubungan spasial asam-asam amino tersebut asan menentukan struktur 3 dimensi dan sifat-sifat biologis protein sederhana.
Sedangkan Protein (akar kata protos dari bahasa Yunani yang berarti “yang paling utama”) adalah senyawa organik kompleks berbobot molekul tinggi yang merupakan polimer dari monomer-monomer asam amino yang dihubungkan satu sama lain dengan ikatan peptida. Molekul protein mengandung karbon, hidrogen, oksigen, nitrogen dan kadang kala sulfur serta fosfor. Protein berperan penting dalam struktur dan fungsi semua sel makhluk hidup dan virus.
Semua protein terdapat dalam semua makhluk hidup, tanpa memandang fungsinya dan aktivitas biologisnya, dibangun oleh susunan dasar yang sama, yaitu 20 asam amino baku, yang molekulnya sendiri tidak mempunyai aktivitas biologis. Lalu apakah yang memberikan suatu protein untuk aktivitas enzimnya, protein lain untuk aktivitas hormon, dan yang lain lagi untuk aktivitas antibodi? Bagaimana kimiawi protein-protein ini berbeda?. Secara cukup sederhana, protein berbeda satu sama lain karena masing-masing mempunyai deret unit asam amino sendiri-sendiri. Asam amino merupakan abjad struktur protein karena molekul-molekul ini dapat disusun dalam sejumlah deret yang hampir tidak terbatas, untuk membuat berbagai protein dalam jumlah yang hampir tidak terbatas pula.
Pengertian Asam Amino
Asam amino yang merupakan monomer (satuan pembentuk) protein adalah suatu senyawa yang mempunyai dua gugus fungsi yaitu gugus amino dan gugus karboksil. Dalam biokimia seringkali pengertiannya dipersempit: keduanya terikat pada satu atom karbon (C) yang sama Gugus karboksil memberikan sifat asam dan gugus amina memberikan sifat basa.
Dalam bentuk larutan, asam amino bersifat amfoterik yaitu cenderung menjadi asam pada larutan basa dan menjadi basa pada larutan asam. Perilaku ini terjadi karena asam amino mampu menjadi zwitter-ion. Asam amino termasuk golongan senyawa yang paling banyak dipelajari karena salah satu fungsinya sangat penting dalam organisme, yaitu sebagai penyusun protein.
Pada asam amino, gugus amino terikat pada atom karbon yang berdekatan dengan gugus karboksil (C-α) atau dapat dikatakan juga bahwa gugus amina dan gugus karboksil dalam asam amino terikat pada atom karbon yang sama.
Struktur Asam Amino
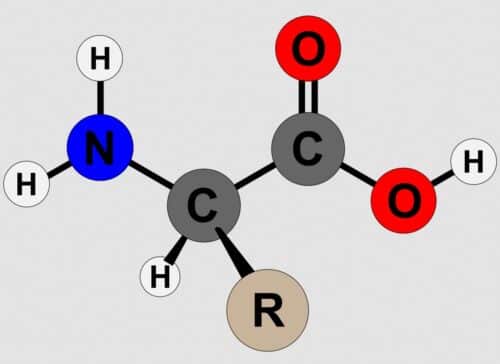
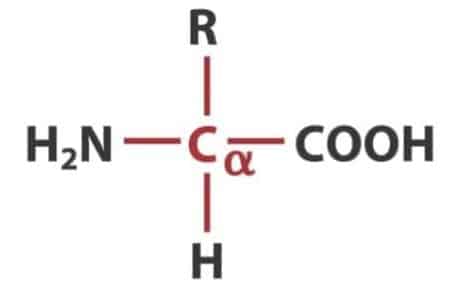
Struktur asam amino secara umum adalah satu atom C yang mengikat empat gugus: gugus amina (NH2), gugus karboksil (COOH), atom hidrogen (H), dan satu gugus sisa (R, dari residue) atau disebut juga gugus atau rantai samping yang membedakan satu asam amino dengan asam amino lainnya. Atom C pusat tersebut dinamai atom Cα (“C-alfa”) sesuai dengan penamaan senyawa bergugus karboksil, yaitu atom C yang berikatan langsung dengan gugus karboksil.
Oleh karena gugus amina juga terikat pada atom Cα ini, senyawa tersebut merupakan asam α-amino. Asam amino biasanya diklasifikasikan berdasarkan sifat kimia rantai samping tersebut menjadi empat kelompok. Rantai samping dapat membuat asam amino bersifat asam lemah, basa lemah, hidrofilik jika polar, dan hidrofobik jika nonpolar.
Baca Juga: Pencemaran Lingkungan adalah
Klasifikasi Asam amino
Asam amino yang terdapat dalam protein dapat dibagi menjadi 4 golongan berdasarkan relatif gugus R-nya.
- Asam amino dengan gugus R non polar (tak mengutup)
Gugus non polar adalah gugus yang mempunyai sedikit atau tidak mempunyai selisih muatan dari daerah yang satu ke daerah yang lain. Golongan ini terdiri dari lima asam amino yang mengandung gugus alifatik (Alanin, leusin, isoleusin, valin,dan prolin) dua dengan R aromatic (fenilalanin dan triptopan) dan satu mengandung atom sulfur (metionin).
- Asam amino dengan gugus R mengutub tak bermuatan
Golongan ini lebih mudah larut dalam air dari golongan yang tak mengutub karena gugus R mengutup dapat membentuk ikatan hydrogen dengan molekul air. Selain treoinin dan tirosin yang kekutubannya disebabkan oleh adanya gugus hidroksil (-OH) merupakan asam amino yang termasuk golongan ini. Selain itu yang termasuk dalam golongan ini juga adalah asparagin dan glutamine yang kekutubannya disebabkan oleh gugus amida (-CONH2) serta sistein oleh gugus sulfidril (-SH).
Asparagin dan glutamine, masing masing merupakan bentuk senyawa amida dari asam aspartat dan asam glutamat dan mudah terhidrolisis oleh asam atau basa. Sistein yang mengandung gugus tiol dan tirosin yang mengandung gugus hidroksil fenol bersifat paling mengutub dalam golongan asam amino ini.
- Asam amino dengan gugus R bermuatan negative (Asam amino asam)
Golongan asam amino ini bermuatan negative pada pH 6.0-7.0 dan terdiri dari asam aspartat dan asam glutamat yang masing-masing mempunyai dua gugus karboksil (COOH).
- Asam amino dengan gugus R bermuatan positif (Asam amino basa)
Golongan asam amino ini bermuatan positif pada pH 7.0 terdiri dari lisin, histidin dan arginin
- Lisin mengandung satu lagi gugus amino pada posisis e dari rantai R alifatik
- Histidin mengandunga gugus lemah imidazolium pada pH 6.0 lebih dari 50 % molekul histidin bermuatan positif sedangkan pada pH 7.0 kurang dari 10 %bermuatan positif.
- Arginin mempunyai gugus guanido pada gugus R-nya.
Berdasarkan biosintesis, Asam Amino diklasifikasikan menjadi tiga jenis, yaitu Asam amino essensial, Asam amino nonessensial dan Asam amino essensial bersyarat.
- Asam amino esensial, adalah asam amino yang tidak bisa diproduksi sendiri oleh tubuh, sehingga harus didapat dari konsumsi makanan. Jenis-jenis Asam amino esensial yaitu : Histidin, Isoleusin, Leusin, Lysin, Metionin, Fenilalanin, Treonin, Triftofan, Valin.
- Asam amino non-esensial adalah asam amino yang bisa diproduksi sendiri oleh tubuh, sehingga memiliki prioritas konsumsi yang lebih rendah dibandingkan dengan asam amino esensial.
- Asam amino esensial bersyarat adalah kelompok asam amino non-esensial, namun pada saat tertentu, seperti setelah latihan beban yang keras, produksi dalam tubuh tidak secepat dan tidak sebanyak yang diperlukan sehingga harus didapat dari makanan maupun suplemen protein.
Sintesis Asam Amino
Semua jaringan memiliki kemampuan untuk men-sintesis asam amino non esensial, melakukan remodeling asam amino, serta mengubah rangka karbon non asam amino menjadi asam amino dan turunan lain yang mengandung nitrogen. Jalur metabolik utama dari asam-asam amino terdiri atas pertama, produksi asam amino dari pembongkaran protein tubuh, digesti protein diet serta sintesis asam amino di hati. Kedua, pengambilan nitrogen dari asam amino. Sedangkan ketiga adalah katabolisme asam amino menjadi energi melalui siklus asam serta siklus urea sebagai proses pengolahan hasil sampingan pemecahan asam amino. Keempat adalah sintesis protein dari asam-asam amino.
Asam amino juga mengalami katabolisme, ada 2 tahap pelepasan gugus amin dari asam amino, yaitu: Transaminasi dan Pelepasan amin dari glutamat menghasilkan ion ammonium.
Tetapi, hati merupakan tempat utama metabolisme nitrogen. Dalam kondisi surplus diet, nitrogen toksik potensial dari asam amino dikeluarkan melalui transaminasi, deaminasi dan pembentukan urea. Rangka karbon umumnya diubah menjadi karbohidrat melalui jalur glukoneogenesis, atau menjadi asam lemak melalui jalur sintesis asam lemak. Berkaitan dengan hal ini, Asam amino dikelompokkan menjadi 3 kategori yaitu:
- Asam amino glukogenik
- ketogenik serta glukogenik, dan
- ketogenik.
Asam amino glukogenik adalah asam-asam amino yang dapat masuk ke jalur produksi piruvat atau intermediat siklus asam sitrat seperti α-ketoglutarat atau oksaloasetat. Semua asam amino ini merupakan prekursor untuk glukosa melalui jalur glukoneogenesis. Semua asam amino kecuali lisin dan leusin mengandung sifat glukogenik. Lisin dan leusin adalah asam amino yang semata-mata ketogenik, yang hanya dapat masuk ke intermediat asetil KoA atau asetoasetil KoA.
Ikatan Peptida
Asam amino untuk membentuk suatu protein dihubungkan dengan ikatan peptida. Dua molekul asam amino dapat diiikat secara kovalen melalui suatu ikatan amida subtitusi yang disebut ikatan peptida menghasilkan suatu dipeptida. Ikatan seperti ini dibentuk dengan menarik unsur H2O dari gugus karboksil satu asam amino dan gugus α-amino dari molekul lain, dengan reaksi kondensasi yang kuat. 3 asam amino dapat disatukan oleh dua ikatan peptida dengan cara yang sama untuk membentuk suatu tripeptida : tetrapeptida dan pentapeptida. Jika terdapat banyak asam amino yang tergabung dengan cara demikian struktur yang demikian dinamakan polipeptida.
Unit asam amino didalam peptida biasanya disebut residu (rantai ini bukan lagi merupakan asam amino karena telah kehilangan atom hidrogen dari gugus amino dan sebagian gugus karboksilnya). Residu asam amino pada ujung suatu peptida yang mempunyai gugus α-amino bebas disebut residu terminal amino (juga residu terminal N) : residu pada ujung yang satu lagi, yang mempunyai gugus karboksil bebas disebut terminal karboksil atau residu terminal C. Peptida dimnamakan dari deret kandungan asam amino, dimulai dari residu termina N.
Peran Asam Amino
Selain berperan menghasilkan energi, Asam amino dalam pembentukan protein yang dibutuhkan, pembentuk glukosa, molekul nonprotein (derivat asam amino), badan-badan keton, dll
Baca Juga: Pengetahuan Tentang Jaringan Tumbuhan
Jenis Asam Amino
Secara umum asam amino dibagi menjadi dua bagian besar yakni asam amino esensial dan non esensial. Asam esensial diperlukan oleh tubuh namun tidak dapat diproduksi sendiri oleh tubuh, sedangkan asam amino non esensial bisa dibentuk sendiri oleh tubuh.
Jenis Asam Amino Esensial
Adapun jenis asam amino esensial yaitu:
- Leusin
Untuk kecerdasan, perkembangan otak dan tubuh anak, jenis asam amino ini juga mampu mengatur kadar gula dan keseimbangan nitrogen dalam tubuh. - Lisin
Berfungsi dalam mengatur dan menyebarkan vitamin B3 serta membantu melawan virus dan racun yang masuk ke dalam tubuh. - Isoleusin
Untuk pembentukan otot dan sumber energi tubuh, jenis asam amino ini juga berfungsi mencegah kelainan dan kerusakan sel jaringan tubuh. - Valin
Valin berfungsi dalam pengendalian kekuatan otot tubuh, mengatur jaringan dan pembuluh darah. - Treonin
Mengatur dan mengolah nutrisi yang masuk ke dalam tubuh. - Histidin
Jenis asam amino yang berfungsi dalam pertumbuhan dan perkembangan otak bayi, mengatasi alergi, menjaga kesehatan syaraf, membantu mengeluarkan racun dan kesehatan reproduksi. - Fenilalanin
Mengatur mood dengan cara mengelola protein dan zat kimia yang masuk ke dalam tubuh. - Triptofan
Mengatur mood dengan cara mengelola protein dan zat kimia yang masuk ke dalam tubuh. - Metionin
Mengatur zat kolin dan kreatin.
Jenis Asam Amino Non Esensial
Adapun jenis asam amino non esensial yaitu:
- Alanin
Alanin ini digambarkan sebagai pembentuk otot dan penghasil energi tubuh, alanin juga berfungsi dalam pembentukan kekebalan tubuh. - Arginin
Arginin fungsinya untuk meregenerasi sel dan jaringan tubuh, jadi asam amino jenis ini sangat diperlukan dalam penyembuhan luka, juga berfungsi dalam produksi hormon pertumbuhan badan dan sistem imunitas tubuh. - Asparagin
Jenis asama amino yang berfungsi dalam keseimbangan syaraf, mengurangi kelelahan tubuh, sistem imun dan berperan dalam sintesis DNA. - Asam Aspartat
Asam amino yang berfungsi dalam meningkatkan stamina tubuh, pembentukan antibodi, peningkatan aktivitas enzim dan melindungi organ hati. - Sistein
Sistein berfungsi sebagai antioksidan, pelindung tubuh dari radikal bebas, senyawa penyehat rambut, untuk pertumbuhan dan regenarasi kulit. Jenis asam amino ini termasuk yang mengandung sulfur. - Asam Glutamat
Jenis asam amino sangat berperan penting dalam mengangkut glutamat dan asam amino dalam darah. Asam glutamat juga membantu dalam proses penyembuhan luka dan mengurangi resiko kerusakan sel otak. - Glutamin
Glutamin berfungsi untuk kekebalan tubuh, anti depresi, berperan dalam sistem pencernaan dan terlibat pada proses sintesis DNA. - Glisin
Glisin membentuk sel darah merah, merupakan bagian dari enzim yang menghasilkan energi dan terlibat pada proses metabolisme glikogen. - Prolin
Berperan penting dalam mempengaruhi tingkat gizi seseorang, prolin ialah komponen dalam penyusunan tulang rawan dan sendi, prolin juga berfungsi dalam menjaga otot jantung. - Serin
Serin berperan penting dalam metabolisme lemak, pembentukan jaringan tubuh dan pembentukan imunitas. - Tirosin
Tirosin dapat berfungsi mengurangi lemak dan mengendalikan nafsu makan.
Sumber Makanan Asam Amino
Adapun sumber makanan asam amino yang diantaranya yaitu:
- Putih telur
- Daging Kalkun
- Domba
- Kepiting
- Ayam
- Ikan tuna
- Kedelai
- Ikad kod
- Rumput laut
- Dan lain-lain
Baca Juga: Pengertian Dan Fungsi Jaringan Epidermis Menurut Ahli Biologi
Manfaat Asam Amino Secara Umum
Adapun manfaat asam amino secara umum yang diantaranya yaitu:
- Untuk pertumbuhan tubuh
- Kecerdasan otak
- Penyembuhan luka
- Pembentukan enzim dan hormon
- Membentuk otot tubuh
- Mengontrol gula darah
- Mengontrol metabolisme tubuh
- Dan lain-lain
Akibat Kekurangan Protein Asam Amino
Adapun akibat kekurangan protein asam amino yang diantaranya yaitu:
- Mudah kelelahan
- Kurang konsentrasi
- Luka sulit sembuh
- Mudah terserang penyakit
- Kadar gula tidak menentu
- Organ tubuh mudah sakit
- Tulang mudah keropos
- Otot kurang berenergi
- Dan lain-lain
Agar metabolisme dan kesehatan tubuh tetap terjaga, penuhi asupan protein asam amino secara rutin. Asam amino bersifat mudah hilang dan tidak dapat bertahan lama dalam tubuh. Jadi sebaiknya setiap hari mengkonsumsi makanan yang banyak mengandung asama amino.
Pengertian Protein
Protein tersusun dari berbagai asam amino yang masing-masing dihubungkan dengan ikatan peptida. Meskipun demikian, pada awal pembentukannya protein hanya tersusun dari 20 asam amino yang dikenal sebagai asam amino dasar atau asam amino baku atau asam amino penyusun protein (proteinogenik). Asam-asam amino inilah yang disandi oleh DNA/RNA sebagai kode genetik.
Protein berasal dari kata protos (bahasa Yunani) yang berarti “yang paling utama”. Protein adalah senyawa organik kompleks berbobot molekul tinggi yang merupakan polimer dari monomer-monomer asam amino yang dihubungkan satu sama lain dengan ikatan peptida. Molekul protein mengandung karbon, hidrogen, oksigen, nitrogen dan kadang kala sulfur serta fosfor. Protein terdapat pada semua sel hidup, kira-kira 50% dari berat keringnya dan berfungsi sebagai pembangun struktur, biokatalis, hormon, sumber energy, penyangga racun, pengatur pH, dan sebagai pembawa sifat turunan dari generasi ke generasi. Protein berperan penting dalam struktur dan fungsi semua sel makhluk hidup dan virus.
Kebanyakan protein merupakan enzim atau subunit enzim. Jenis protein lain berperan dalam fungsi struktural atau mekanis, seperti misalnya protein yang membentuk batang dan sendi sitoskeleton. Protein terlibat dalam sistem kekebalan (imun) sebagai antibodi, sistem kendali dalam bentuk hormon, sebagai komponen penyimpanan (dalam biji) dan juga dalam transportasi hara. Sebagai salah satu sumber gizi, protein berperan sebagai sumber asam amino bagi organisme yang tidak mampu membentuk asam amino tersebut (heterotrof).
Baca Juga: Anatomi Tumbuhan Alga Menurut Ahli Biologi
Protein merupakan salah satu dari biomolekul raksasa, selain polisakarida, lipid, dan polinukleotida, yang merupakan penyusun utama makhluk hidup. Selain itu, protein merupakan salah satu molekul yang paling banyak diteliti dalam biokimia. Protein ditemukan oleh Jöns Jakob Berzelius pada tahun 1838.
Biosintesis protein alami sama dengan ekspresi genetik. Kode genetik yang dibawa DNA ditranskripsi menjadi RNA, yang berperan sebagai cetakan bagi translasi yang dilakukan ribosom. Sampai tahap ini, protein masih “mentah”, hanya tersusun dari asam amino proteinogenik. Melalui mekanisme pascatranslasi, terbentuklah protein yang memiliki fungsi penuh secara biologi.
Struktur Protein
- Struktur tersier protein. Protein ini memiliki banyak struktur sekunder beta-sheet dan alpha-helix yang sangat pendek. Model dibuat dengan menggunakan koordinat dari Bank Data Protein.
- Struktur protein dapat dilihat sebagai hirarki, yaitu berupa struktur primer (tingkat satu), sekunder (tingkat dua), tersier (tingkat tiga), dan kuartener (tingkat empat).
- Struktur primer protein merupakan urutan asam amino penyusun protein yang dihubungkan melalui ikatan peptida (amida). Frederick Sanger merupakan ilmuwan yang berjasa dengan temuan metode penentuan deret asam amino pada protein, dengan penggunaan beberapa enzim protease yang mengiris ikatan antara asam amino tertentu, menjadi fragmen peptida yang lebih pendek untuk dipisahkan lebih lanjut dengan bantuan kertas kromatografik. Urutan asam amino menentukan fungsi protein, pada tahun 1957, Vernon Ingram menemukan bahwa translokasi asam amino akan mengubah fungsi protein, dan lebih lanjut memicu mutasi genetik.
Struktur primer protein bisa ditentukan dengan beberapa metode:
- Hidrolisis protein dengan asam kuat (misalnya, 6N HCl) dan kemudian komposisi asam amino ditentukan dengan instrumen amino acid analyzer,
- Analisis sekuens dari ujung-N dengan menggunakan degradasi Edman,
- Kombinasi dari digesti dengan tripsin dan spektrometri massa, dan
- Penentuan massa molekular dengan spektrometri massa.
- Struktur sekunder protein adalah struktur tiga dimensi lokal dari berbagai rangkaian asam amino pada protein yang distabilkan oleh ikatan hidrogen.
Struktur sekunder bisa ditentukan dengan menggunakan spektroskopi circular dichroism (CD) dan Fourier Transform Infra Red (FTIR). Spektrum CD dari puntiran-alfa menunjukkan dua absorbans negatif pada 208 dan 220 nm dan lempeng-beta menunjukkan satu puncak negatif sekitar 210-216 nm. Estimasi dari komposisi struktur sekunder dari protein bisa dikalkulasi dari spektrum CD. Pada spektrum FTIR, pita amida-I dari puntiran-alfa berbeda dibandingkan dengan pita amida-I dari lempeng-beta. Jadi, komposisi struktur sekunder dari protein juga bisa diestimasi dari spektrum inframerah.
- Struktur tersier yang merupakan gabungan dari aneka ragam dari struktur sekunder. Struktur tersier biasanya berupa gumpalan. Beberapa molekul protein dapat berinteraksi secara fisik tanpa ikatan kovalen membentuk oligomer yang stabil (misalnya dimer, trimer, atau kuartomer) dan membentuk struktur kuartener.
- Struktur kuartener, contoh dari struktur ini yang terkenal adalah enzim Rubisco dan insulin.
Struktur protein lainnya yang juga dikenal adalah domain. Struktur ini terdiri dari 40-350 asam amino. Protein sederhana umumnya hanya memiliki satu domain. Pada protein yang lebih kompleks, ada beberapa domain yang terlibat di dalamnya.
Hubungan rantai polipeptida yang berperan di dalamnya akan menimbulkan sebuah fungsi baru berbeda dengan komponen penyusunnya. Bila struktur domain pada struktur kompleks ini berpisah, maka fungsi biologis masing-masing komponen domain penyusunnya tidak hilang. Inilah yang membedakan struktur domain dengan struktur kuartener. Pada struktur kuartener, setelah struktur kompleksnya berpisah, protein tersebut tidak fungsional
Baca Juga: Antioksidan Adalah
Proses Pembentukan Protein
Proses pembentukan protein terjadi melalui 2 proses utama, yaitu Transkripsi dan Translasi. Transkripsi (proses sintesa RNA dari DNA menghasilkan mRNA). Translasi (proses pembentukan polipeptida dari mRNA hasil Transkripsi).
-
Transkripsi
Tahap transkripsi ini mengalami proses utama: Inisiasi, Elongasi, Terminasi.
- Inisiasi
RNA polymerase melekat pada promoter. RNA polymerase membuka strand DNA. RNA nukleotida menempel pada DNA
Template. RNA polymerase menghubungkan RNA nukleotida.
- Elongasi
RNA polymerase bergerak di sepanjang DNA, Nukleotida melekat pada DNA template, Strand RNA mengelupas dari DNA, DNA kembali menyatu.
- Terminasi
RNA polymerase megenai terminator, RNA polymerase melepaskan RNA, RNA polymerase meninggalkan DNA.
-
Translasi
Tahap translasi mengalami proses, yaitu : Inisiasi,Elongasi, Terminasi.
- Inisiasi
Sub unit Ribosom Kecil melekat pada mRNA. Anti kodon tRNA melekat pada Start Kodon. Sub unit Ribosom besar melekat pada sub unit Ribosom kecil.
- Elongasi
Kodon pada sisi A Ribosom, berpasangan dengan anti kodon dari tRNA yang sesuai. Ikatan peptida antara Asam Amino. tRNA melekat pada tRNA selanjutnya seiring bergeraknya Ribosom
- Terminasi
Ribosom sampai pada stop kodonà tRNA tanpa Asam Amino melekat pada stop kodonàpolipeptida lepas à komponen Ribosom lepas.
Baca Juga: Penjelasan Fungsi Lemak Beserta Jenisnya
Klasifikasi Protein
Klasifikasi protein pada biokimia didasarkan atas fungsi biologinya terdiri atas:
- Enzim, merupakan golongan protein yang terbesar dan paling penting. Kira-kira seribu macam enzim telah diketahui, yang masing-masing berfungsi sebagai katalisator reaksi kimia dalam jasad hidup. pada jasad hidup yang berbeda terdapat macam jenis enzim yang berbeda pula. Molekul enzim biasanya berbentuk bulat (globular), sebagian terdiri atas satu rantai polipeptida dan sebagian lain terdiri lebih dari satu polipeptida. Contoh enzim: ribonuklease, suatu enzim yang mengkatalisa hidrolisa RNA (asam poliribonukleat); sitokrom, berperan dalam proses pemindahan electron; tripsin; katalisator pemutus ikatan peptida tertentu dalam polipeptida.
- Protein Pembangun, berfungsi sebagai unsure pembentuk struktur. Beberapa contoh misalnya: protein pembukus virus, merupakan selubung pada kromosom; glikoprotein, merupakan penunjang struktur dinding sel; struktur membrane, merupakan protein komponen membran sel; α-Keratin, terdapat dalam kulit, bulu ayam, dan kuku; sklerotin, terdapat dalam rangka luar insekta; fibroin, terdapat dalam kokon ulat sutra; kolagen, merupakan serabut dalam jaringan penyambung; elastin, terdapat pada jaringan penyambung yang elastis (ikat sendi); mukroprotein, terdapat dalam sekresi mukosa (lendir).
- Protein Kontraktil, merupakan golongan protein yang berperan dalam proses gerak. Sebagai contoh misalnya; miosin, merupakan unsur filamen tak bergerak dalam myofibril; dinei, terdapat dalam rambut getar dan flagel (bulu cambuk).
- Protein Pengangkut, mempunyai kemampuan mengikat molekul tertentu dan melakukan pengangkutan berbagai macam zat melalui aliran darah. Sebagai contoh misalnya: hemoglobin, terdiri atas gugus senyawa heme yang mengandung besi terikat pada protein globin, berfungsi sebagai alat pengangkut oksigen dalam darah vertebrata; hemosianin, befungsi sebagai alat pengangkut oksigen dalam darah beberapa macam invertebrate; mioglobin, sebagai alat pengangkut oksigen dalam jaringan otot; serum albumin, sebagai alat pengangkut asam lemak dalam darah; β-lipoprotein, sebagai alat pengangkut lipid dalam darah; seruloplasmin, sebagai alat pengangkut ion tembaga dalam darah.
- Protein Hormon, termasuk protein yang aktif. Sebagai contoh misalnya: insulin, berfungsi mengatur metabolisme glukosa, hormon adrenokortikotrop, berperan pengatur sintesis kortikosteroid; hormon pertumbuhan, berperan menstimulasi pertumbuhan tulang.
- Protein Bersifat Racun, beberapa protein yang bersifat racun terhadap hewan kelas tinggi yaitu misalnya: racun dari Clostridium botulimum, menyebabkan keracunan bahan makanan; racun ular, suatu protein enzim yang dapat menyebabkan terhidrolisisnya fosfogliserida yang terdapat dalam membrane sel; risin, protein racun dari beras.
- Protein Pelindung, umumnya terdapat dalam darah vertebrata. Sebagai contoh misalnya: antibody merupakan protein yang hanya dibentuk jika ada antigen dan dengan antigen yang merupakan protein asing, dapat membentuk senyawa kompleks; fibrinogen, merupakan sumber pembentuk fibrin dalam proses pembekuan darah; trombin, merupakan komponen dalam mekanisme pembekuan darah.
- Protein Cadangan disimpan untuk berbagai proses metabolisme dalam tubuh. Sebagai contoh, misalnya: ovalbumin, merupakan protein yangterdapat dalam putih telur; kasein, merupakan protein dalam biji jagung.
Baca Juga: Penjelasan Macam-Macam Mineral Beserta Fungsinya
Berdasarkan bentuknya, protein dikelompokkan sebagai berikut :
-
Protein bentuk serabut (fibrous)
Protein ini terdiri atas beberapa rantai peptida berbentu spiral yang terjalin. Satu sama lain sehingga menyerupai batang yang kaku. Karakteristik protein bentuk serabut adalah rendahnya daya larut, mempunyai kekuatan mekanis yang tinggi untuk tahan terhadap enzim pencernaan. Kolagen merupakan protein utama jaringan ikat. Elasti terdapat dalam urat, otot, arteri (pembuluh darah) dan jaringan elastis lain. Keratini adalah protein rambut dan kuku. Miosin merupakan protein utama serat otot.
-
Protein Globuler
Berbentuk bola terdapat dalam cairan jaringan tubuh. Protein ini larut dalam larutan garam dan encer, mudah berubah dibawah pengaruh suhu, konsentrasi garam dan mudah denaturasi. Albumin terdapat dalam telur, susu, plasma, dan hemoglobin. Globulin terdapat dalam otot, serum, kuning telur, dan gizi tumbuh-tumbuhan. Histon terdapat dalam jaringan-jaringan seperti timus dan pancreas. Protamin dihubungkan dengan asam nukleat.
-
Protein Konjugasi
Merupakan protein sederhana yang terikat dengan baha-bahan non-asam amino. Nukleoprotein terdaoat dalam inti sel dan merupakan bagian penting DNA dan RNA. Nukleoprotein adalah kombinasi protein dengan karbohidrat dalam jumlah besar. Lipoprotein terdapat dalam plasma-plasma yang terikat melalui ikatan ester dengan asam fosfat sepertu kasein dalam susu. Metaloprotein adalah protein yang terikat dengan mineral seperti feritin dan hemosiderin adalah protein dimana mineralnya adalah zat besi, tembaga dan seng.
Sintesis Protein
Dari makanan kita memperoleh Protein. Di sistem pencernaan protein akan diuraikan menjadi peptid peptid yang strukturnya lebih sederhana terdiri dari asam amino. Hal ini dilakukan dengan bantuan enzim. Tubuh manusia memerlukan 9 asam amino. Artinya kesembilan asam amino ini tidak dapat disintesa sendiri oleh tubuh esensiil, sedangkan sebagian asam amino dapat disintesa sendiri atau tidak esensiil oleh tubuh. Keseluruhan berjumlah 21 asam amino. Setelah penyerapan di usus maka akan diberikan ke darah. Darah membawa asam amino itu ke setiap sel tubuh. Kode untuk asam amino tidak esensiil dapat disintesa oleh DNA. Ini disebut dengan DNAtranskripsi. Kemudian mRNA hasil transkripsi di proses lebih lanjut di ribosom atau retikulum endoplasma, disebut sebagai translasi.
Baca Juga: 11 Vitamin Serta Fungsi, Jenis, Sumber Dan Akibat Kekurangannya Lengkap
Peran protein
Protein adalah komponen terbesar dalam tubuh manusia setelah air. Jumlahnya 1/6 dari berat tubuh manusia, dan tersebar di dalam otot, tulang, kulit, serta berbagai cairan tubuh. Protein sangat diperlukan tubuh, fungsi utamanya sebagai zat pembangun sangat diperlukan pada masa pertumbuhan. Pada masa bayi hingga remaja, kebutuhan protein lebih besar persentasenya dibandingkan dengan pada masa dewasa dan manula. Pada masa dewasa dan manula protein dibutuhkan untuk mempertahankan jaringan-jaringan tubuh dan mengganti sel-sel yang telah rusak. Selain itu protein juga memiliki fungsi lain yaitu:
- Sebagai enzim
Hampir semua reaksi biologis dipercepat atau dibantu oleh suatu senyawa makromolekul spesifik yang disebut enzim, dari reaksi yang sangat sederhana seperti reaksi transportasi karbon dioksida sampai yang sangat rumit seperti replikasi kromosom.
- Alat pengangkut dan penyimpan
Banyak molekul dengan MB kecil serta beberapa ion dapat diangkut atau dipindahkan oleh protein-protein tertentu. Pengatur pergerakan Protein merupakan komponen utama daging, gerakan otot terjadi karena adanya dua molekul protein yang saling bergeseran.
- Penunjang mekanis
Kekuatan dan daya tahan robek kulit dan tulang disebabkan adanya kolagen, suatu protein berbentuk bulat panjang dan mudah membentuk serabut. Pertahanan tubuh atau imunisasi pertahanan tubuh biasanya dalam bentuk antibodi, yaitu suatu protein khusus yang dapat mengenal dan menempel atau mengikat benda-benda asing yang masuk ke dalam tubuh seperti virus, bakteri, dan sel- sel asing lain.
- Media perambatan impuls syaraf
Protein yang mempunyai fungsi ini biasanya berbentuk reseptor, misalnya rodopsin, suatu protein yang bertindak sebagai reseptor penerima warna atau cahaya pada sel-sel mata.
- Pengendalian pertumbuhan
Protein ini bekerja sebagai reseptor (dalam bakteri) yang dapat mempengaruhi fungsi bagian-bagian DNA yang mengatur sifat dan karakter bahan.
Baca Juga: Penjelasan Protein Serta Fungsi, Sumber Dan Akibat Kekurangannya Lengkap
Manfaat Protein dan Asam Amino dalam bidang Farmasi
Kemajuan teknologi DNA rekombinan telah mendorong perkembangan berbagai cara produksi protein rekombinan menggunakan inang yang aman dan relatif mudah dikultur sehingga protein dapat diproduksi pada skala industri. Protein yang digunakan untuk bidang farmasi dan kedokteran (protein terapeutik dan vaksin subunit) disyaratkan mempunyai kemurnian yang tinggi. Teknologi DNA rekombinan juga telah menyediakan berbagai strategi untuk meningkatkan produksi dan mempermudah pemurnian protein.
Mutu protein juga sangat penting, oleh karena itu telah dikembangkan berbagai metode identifikasi dan karakterisasi protein menggunakan metode berbasis protein, diantaranya: sekuensing urutan asam amino, elektroforesis dan imunobloting, penentuan pH isoelektrik, dan spektrometri massa MALDI-TOF. Dalam bidang farmasi terutama untuk penyakit kanker, protein rekombinan termasuk antibodi monoklonal juga digunakan dalam sistem penghantaran obat dengan tujuan untuk peningkatan efektivitas dan penurunan efek toksik dari obat.
Salah satu vaksin manusia dan hewan yang saat ini banyak dikembangkan adalah vaksin subunit yang terdiri atas protein rekombinan. Selain di bidang farmasi dan kedokteran, protein rekombinan juga telah digunakan di berbagai industri lain seperti makanan-minuman, kosmetik (Botox), lingkungan, dan pertanian.
DAFTAR PUSTAKA
Adnyana, Putu. 2012. Makalah Asam Amino. http://www.scribd.com/doc/19875984/XIIIXIV-Asam amino. diakses pada tanggal 27 September 2012.
Ardiyan, Agusta: 28 Juni 2012. MAKALAH BIOKIMIA : PROTEIN. http://www.clickardiyan.blogspot.com/2012/06/makalah-biokimia-protein.html . Diakses pada tanggal 30 September 2012.
D.W.Martin,Jr. and P.A.Mayes and V.W.Rodwell.BIOKIMIA (Review of Biochemistry).Terjemahan Penerbit Buku Kedokteran E.G.
Harold Hart,” Organic Chemistry” a Short Course, Sixth Edition, Michigan State University, 1983, Houghton Mifflin Co.
Lehninger, Albert L., Dasar-dasar Biokimia Jilid 1, Erlangga, 1982, Jakarta.
Ralp J. Fessenden and Joan S. Fessenden, “ Organic Chemistry,” Third Edition, University Of Montana, 1986, Wadsworth, Inc, Belmont, Califfornia 94002, Massachuset, USA.
Suharsono.1988,Biokimia Jilid 1.UGM PRESS : Jogjakarta.
Unja, of Chemistry. 2011. KLASIFIKASI DAN FUNGSI PROTEIN. http://www.kimia-master.blogspot.com/2011/11/klasifikasi-dan-fungsi-protein.hmtl/ . diakses pada tanggal 29 September 2012.
Demikianlah pembahasan mengenai Asam Amino Adalah – Pengertian, Makalah Penggolongan Dan Sifatnya semoga dengan adanya ulasan tersebut dapat menambah wawasan dan pengetahuan kalian semua,, terima kasih banyak atas kunjungannya. 🙂 🙂 🙂