Daftar isi biasanya terdapat pada karya ilmiah, skripsi, buku, dan sebagainya. Dalam membuat daftar isi ini bisa dilakukan dengan melalui banyak cara. Misalnya dengan menggunakan word baik dalam versi 2007, 2010, 2013, 2016 maupun 2019. Cara membuat titik-titik daftar isi dengan word sangat mudah.
Titik-titik dalam daftar isi dibuat supaya tampilan pada halaman daftar isi terlihat lebih rapi. Ternyata cara pembuatannya pun tidak sulit jika Anda menggunakan Ms. Word. Anda bisa mempraktekannya di rumah dengan Ms. Word versi apapun yang Anda miliki.
Apa itu Daftar Isi?
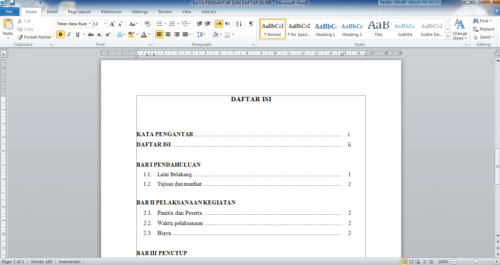
Susunan dari judul-judul dan juga subjudul yang terdapat pada isi buku, makalah dan karya tulis lainnya disebut dengan daftar isi. Biasanya letak dari daftar isi ini ada di bagian awal buku, makalah dan sebagainya.
Apa Fungsi Daftar Isi?
Fungsi dari daftar isi itu sendiri adalah sebagai petunjuk untuk para pembaca, agar mereka bisa menemukan letak halaman atau subjudul dari buku tersebut dengan hanya melihat bagian daftar isinya saja. Pembaca pun tak harus mencari halaman di dalam buku satu per satu.
Tak ada bentuk baku dalam pembuatan daftar isi ini. Namun catatan penting dari dibuatnya daftar isi adalah tingkat kerapihannya sendiri. Ditambah dengan susunan pada sub headingnya juga harus jelas, dan jangan membuat pembaca bingung dengan daftar isi tersebut.
Titik-titik penghubung antara judul dengan sub judul dan nomor halaman yang ada pada daftar isi, juga harus rapi dan jelas. Membuat titik-titik daftar isi juga bisa dilakukan secara manual, tetapi biasanya hasilnya akan menjadi kurang rapi.
Akan ada angka halaman yang menjadi tidak rata pada bagian kanan sehingga titik-titiknya menjadi tidak jelas. Itulah sebabnya Anda harus membuat titik-titik pada daftar isi dengan cara otomatis agar hasilnya memuaskan.
Cara Membuat Titik-titik Daftar Isi Agar Lebih Rapi (Manual)
Ada beberapa langkah yang harus Anda lalui dalam membuat titik daftar isi tersebut. Berikut ini cara membuat titik-titik daftar isi yang baik, benar dan juga rapi:
- Buka aplikasi Ms. Word terlebih dahulu.
- Pastikan Anda sudah mengaktifkan rulernya. Cara mengaktifkannya yaitu dengan masuk ke menu View, lalu ke submenu Show, kemudian centang Ruler.
- Setelah itu buat susunan kerangka pada daftar isi yang akan Anda buat nanti.
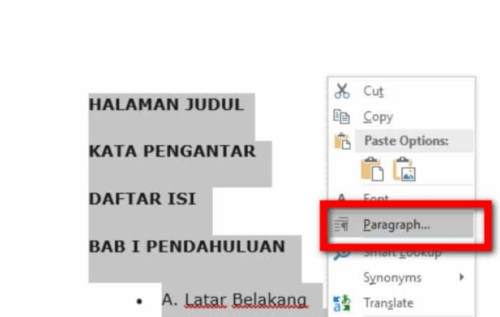
- Lalu blok seluruh kerangka daftar isi yang sudah Anda buat.
- Selanjutnya pilih salah satu opsi seperti berikut ini:
- Klik kanan dan pilih Paragraph, dengan kondisi kerangka daftar isi yang masih terblok.
- Lalu klik tombol kecil yang ada di menu Home dan Paragraph.
- Nanti akan muncul Pop Up dan pilihlah tombol Tabs.
- Nanti akan muncul kembali Pop Up.
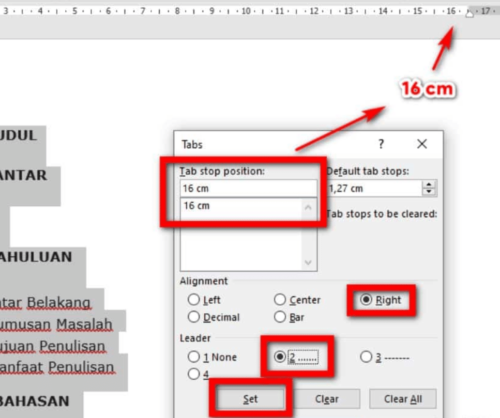
- Lihat kolom Tab Stop Position, di sana Anda harus mengetikkan bagian tepi ujung untuk posisi rata kanan. Sebaiknya sisakan ukuran 0,5 jangan terlalu pas.
- Untuk bagian Alignment pilih saja Right untuk membuat rata kanan.
- Pada bagian Leader Anda harus pilih 2 supaya terlihat titik-titik di sana.
- Kemudian klik lagi tombol Set, supaya ujung rata kanannya bisa menjadi referensi Opsional di masa mendatang.
- Klik tombol
- Kemudian arahkan kursor ke arah ujung pada kerangka kalimat di daftar isi yang sudah Anda buat. Lalu tekan juga tombol Tab di keyboard.
- Nantinya titik-titik akan keluar dengan otomatis dan akan berhenti di ujung tepi kanan yang sesuai dengan apa yang sudah Anda atur sebelumnya.
- Ulangi lagi langkah di poin 8 hingga seluruh titik-titik pada kerangka daftar isi sudah terisi.
- Pada ujung rata kanan, pembuatan titik-titik bisa dengan mengulang poin nomor 5, dan saat sudah berada di poin ke 7 Anda bisa mengubah kolom Tab Stop Position. Rumusnya yaitu mula-mula + 0.5. Langkah selanjutnya yaitu pilih Leader di 1 None supaya tak ada titik-titik lagi.
Pada poin ke 8 tadi, Anda bisa langsung mengetikkan posisi halaman jika tombol Tab sudah ditekan.
Keunggulan dalam Membuat Daftar Isi Secara Otomatis
Seperti yang telah dijelaskan sebelumnya, ada dua pilihan yang bisa dipilih ketika Anda akan membuat titik-titik daftar isi yaitu cara manual dan otomatis. Namun, lebih banyak orang yang memilih cara membuat titik-titik daftar isi secara otomatis karena memiliki sejumlah keunggulannya sendiri.
Salah satu keunggulan dari menggunakan cara otomatis ini adalah Anda tak perlu mengedit lagi daftar isi apabila ingin menambahkan bagian/halaman yang baru. Cukup dengan menambahkan bagian headingnya saja, maka daftar isinya akan muncul secara otomatis.
Hal itu akan lebih menghemat waktu Anda sehingga lebih efektif dan efisien.
Cara Menambah Daftar Isi (Update Daftar Isi)
Berikut ini cara menambah daftar isi secara otomatis, sehingga Anda tidak usah repot mengedit bagian-bagiannya:
- Pilih dahulu halaman mana yang akan Anda tambahkan untuk bagian pentingnya.
- Misalnya ketika Anda ingin menambahkan halaman paling akhir di tab Home, langsung saja klik Heading yang dibutuhkan kemudian tulis juga teksnya.
- Bagian yang tadi Anda jadikan Heading akan muncul dengan otomatis di daftar isi.
- Selesai.
Pengaturan Judul dalam Membuat Daftar Isi
Cara mudah dalam membuat judul pada setiap bab yang ada di buku, makalah, karya tulis dan yang lainnya di dalam paragraf adalah, dengan membesarkan ukuran hurufnya. Cara itu memang benar dan bisa dilakukan, tapi agaknya kurang tepat.
Aplikasi pada Ms. Word memiliki pengaturan yang tepat dalam hal gaya judul, mulai dari judul di dalam buku hingga bagian subjudulnya. Sistemnya hampir sama dengan membuat judul pada website. Judul dengan subjudul akan merujuk pada judul utama sebuah karya tulis itu sendiri.
Sedangkan judul yang ada di daftar isi meliputi Heading 1, 2, 3, dan 4.
Anda juga memperbaharui kembali daftar isi yang telah Anda buat tadi. Perbaharuan daftar isi ini pun bisa dilakukan dengan cara otomatis, yaitu dengan cara berikut ini:
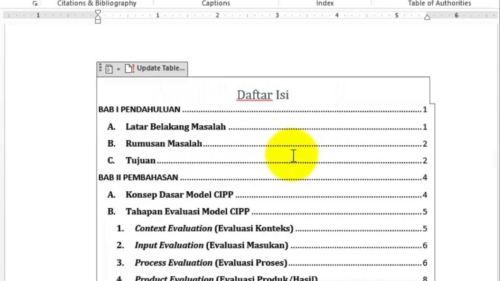
- Untuk mengaktifkannya klik saja daftar isi yang sudah Anda buat.
- Klik kembali tombol berbentuk panah yang ada di bagian atas kotak Table of Content.
- Setelah itu klik lagi Perbarui atau Update.
- Hasil dari perbaruan daftar isi ini akan sama dengan edit daftar isi yang sesuai dengan yang Anda buat tadi.
Cara membuat titik-titik daftar isi yang sudah diuraikan di atas memang sangat mudah, karena dibantu oleh aplikasi Ms. Word. Maka Anda bisa membuat daftar isi pada buku, makalah atau karya tulis lainnya yang Anda buat dengan mudah dan cepat.
Hal ini akan sangat memengaruhi cara kerja Anda dan tingkat efektivitas pada waktu pembuatannya pun lebih praktis dan efisien. Itulah sebabnya cara membuat titik-titik daftar isi ini lebih direkomendasikan cara otomatis.
Lihat Juga :